- · 《临床心电学杂志》期刊[01/26]
- · 《临床心电学杂志》投稿[01/26]
- · 临床心电学杂志版面费是[01/26]
新冠疫苗刚获巴西临床试验,尚无商业化产品,
作者:网站采编关键词:
摘要:记者 | 郭净净 随着各地疫情反复,各家疫苗公司正在加紧疫苗研发工作。近日,四川三叶草生物制药有限公司(Clover Biopharmaceuticals,下称“三叶草生物”)向港交所递交上市申请材料
记者 |郭净净
随着各地疫情反复,各家疫苗公司正在加紧疫苗研发工作。近日,四川三叶草生物制药有限公司(Clover Biopharmaceuticals,下称“三叶草生物”)向港交所递交上市申请材料,高盛、中金公司担任联席保荐人。
招股书显示,三叶草生物是一家临床阶段生物技术公司,致力于开发新型疫苗及生物治疗候选产品,解决全球最危及生命的疾病及公共卫生威胁。
该公司称,其将有望成为首批在全球范围内商业化COVID-19重组蛋白疫苗的公司之一。据巴西卫生监督局4月19日公布,已于4月16日批准由三叶草生物研发的一款新冠疫苗在该国进行Ⅱ期和Ⅲ期临床试验;这款疫苗需要间隔21天接种两剂。这是第二款获批在巴西进行临床试验的中国新冠疫苗。
三叶草生物称,该公司的临床前小鼠免疫原性研究表明其单价南非变种(SARS-CoV-2的B.1.351变种)候选疫苗有可能会广泛用于预防当前流行的原始SARS-CoV-2毒株及变种。
招股书显示,在取得SPECTRA的中期数据后,该公司计划于2021年下半年向EMA、国家药监局及世界卫生组织提交有条件的监管审批申请,并计划于2021年年底前启动产品上市。

三叶草生物还称,其潜在最大产能每年自主生产超过10亿剂SCB-2019;预期将在全球范围内商业化首批COVID-19重组蛋白疫苗中的其中一款,有望帮助解决全球COVID-19疫苗短缺的问题,并抢占直至2026年前全球需要约150亿剂COVID-19疫苗(假设疫苗方案为两剂次及考虑全球政府的采购及储备)带来的重要市场份额。
此外,据介绍,该公司独有的Trimer-Tag?专利技术平台是研制新型疫苗及生物疗法的产品开发平台。该平台可以三聚体化任何靶蛋白并靶向多种天然依赖于三聚体化的疾病及生物靶点,包括数十种包膜RNA病毒(如冠状病毒、狂犬病、呼吸道合胞病毒(RSV)、流感、艾滋病病毒(HIV)及埃博拉病毒)以及对多种重症疾病(包括若干癌症及自体免疫疾病)等。
截至最后实际可行日期,三叶草生物的的产品管线包括(i)六种Trimer-Tag?亚单位候选疫苗、两种Trimer-Tag?肿瘤候选产品及三种Fc融合候选产品,涵盖13种适应症。此外,截至同日,该公司已启动有九项临床试验。SCB-2019 (CpG 1018加铝佐剂)其核心产品。
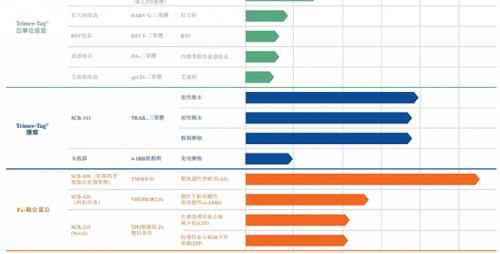
此外,三叶草生物还开发Fc融合蛋白分子及生物仿制药的项目,目前其进度最快的项目是用于治疗风湿性疾病的SCB-808(一款恩利(依那西普)生物仿制药,采用可立即注射的预充式制剂),该产品目前正在中国进行SCB-808的关键性III期临床试验,预期将于2022年向国家药监局提交新药申请,并在获批准后开始商业化。
尽管尚无商业化产品,三叶草生物表示,公司在浙江长兴拥有生物药生产基地,已准备就绪进行商业化生产。该基地已准备好进行SCB-2019快速扩大规模的商业生产。
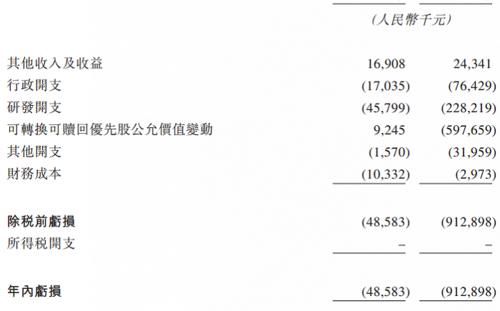
三叶草生物目前暂无销售的产品,也无任何产品销售收入。招股书显示,2019年、2020年,该公司年内亏损额分别是4858.3万元、9.13亿元,其中研发开支分别是4579.9万元、2.28亿元。
招股书显示,三叶草生物此次港股IPO募资将用于核心产品及相关产品的研发、生产及商业化。其中,一个主要募投方向是用于SCB-2019(CpG 1018加铝佐剂)的监管意见书申请、商业化准备及上市;其次,则将用于公司的第二代COVID-19候选疫苗的研发及监管意见书申请;此外,该公司将募资用于SCB-808的研发、商业化准备及上市。
面对新药研发的巨大开支,三叶草生物自成立以来已进行五轮融资。2021年2月,三叶草生物刚完成C轮融资,获得高瓴资本、淡马锡、海松资本、奥博资本、Delos Capital等2.3亿美元投资,招股书显示此轮融资公司的投后估值为9.3亿美元。此前,该公司的投资者还有金龙集团、中关村创投、贝达生物医药产业基金、前海母基金等。最新招股书显示,高瓴资本、淡马锡均跻身三叶草生物前五大股东之列。其中,高瓴资本通过AUT-XXI、JNRY分别持有三叶草生物股份7.82%、10.61%,IPO前合计持股比例约18.43%。
从管理层来看,三叶草生物执行董事为梁朋(60岁)、梁果(29岁),二人均为美国籍。IPO前,梁朋持股为22.19%,梁果持股为1.88%。梁朋为梁果父亲,为公司创始人、董事长兼首席科学官,是Trimer-Tag?技术平台的发明者。据介绍,梁朋知名的科研突破包括发明用于基因表达系统分析的差异显示技术,该技术已由GenHunter Corporation商业化;发现白细胞介素24(IL-24,一种促炎性细胞因子)及其受体,其相关专利权益被惠氏(现“辉瑞公司”)买断。2008年至2009年期间,梁朋曾在范德比尔特大学担任癌症生物学终身副教授。
文章来源:《临床心电学杂志》 网址: http://www.lcxdxzz.cn/zonghexinwen/2021/0517/1010.html
上一篇:信达生物将在2021年美国临床肿瘤学会ASCO年会上公
下一篇:临床超声Venue家族添新丁,为多场景急危时刻临床
临床心电学杂志投稿 | 临床心电学杂志编辑部| 临床心电学杂志版面费 | 临床心电学杂志论文发表 | 临床心电学杂志最新目录
Copyright © 2019 《临床心电学杂志》杂志社 版权所有
投稿电话: 投稿邮箱: